ลุยจิ ริชาร์ดิ 1 , โรซ่า มาซเซโอ 2,* © , แองเจโล ราffอาเล่ มาร์โกตริจิอาโน่ 1 , กุกลิเอลโม เรนัลดี 3 , เปาโล อิโอเวียโน่ 4 วีโต้ ซอนโน่ 1 สเตฟาโน ปาวาน 1 © และ Concetta Lotti 2,*
- 1 ภาควิชาวิทยาศาสตร์ดิน พืช และอาหาร หน่วยพันธุศาสตร์และการปรับปรุงพันธุ์พืช University of Bari, Via Amendola 165/A, 70125 Bari, Italy; luigi.ricciardi@uniba.it (ล.ร.);angelo.marcotrigiano@uniba.it (แขน); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (สพป.)
- 2 Department of the Sciences of Agriculture, Food and Environment, University of Foggia, Via Napoli 25, 71122 ฟอจจา, อิตาลี
- 3 ภาควิชาชีววิทยาศาสตร์ เทคโนโลยีชีวภาพและชีวเวชภัณฑ์ มหาวิทยาลัยบารี Via Orabona 4 70125 บารี อิตาลี guglielmo.rainaldi@uniba.it
- 4 Department of Energy Technologies, Bioenergy, Biorefinery and Green Chemistry Division, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), อิตาลี; paolo.iovieno@enea.it
* สารบรรณ: rosa.mazzao@unifg.it (ม.ม.); concetta.lotti@unifg.it (ซีแอล)
นามธรรม:
หัวหอม (อัลเลียมซีปา L.) เป็นพืชผักที่มีความสำคัญเป็นอันดับสองของโลก และได้รับการชื่นชมอย่างกว้างขวางว่ามีประโยชน์ต่อสุขภาพ แม้ว่าหัวหอมจะมีความสำคัญทางเศรษฐกิจและคุณค่าในฐานะอาหารที่มีประโยชน์ แต่หัวหอมก็ยังได้รับการศึกษาที่ไม่ดีเกี่ยวกับความหลากหลายทางพันธุกรรม ในที่นี้ เราได้สำรวจความผันแปรทางพันธุกรรมใน “หัวหอมแดง Acquaviva” (ARO) ซึ่งเป็นพันธุ์ที่มีประวัติการเพาะปลูกมายาวนานนับศตวรรษในเมืองเล็กๆ ในจังหวัด Bari (Apulia ทางตอนใต้ของอิตาลี) มีการใช้ชุดเครื่องหมายไมโครแซทเทลไลท์ 11 ชุดในการสำรวจความผันแปรทางพันธุกรรมในคอลเล็กชันเชื้อโรคที่ประกอบด้วยประชากร ARO 13 ตัวและประเภทการค้าทั่วไปสามประเภท การวิเคราะห์โครงสร้างทางพันธุกรรมด้วยวิธีแบบพาราเมตริกและแบบไม่ใช้พาราเมตริกเน้นว่า ARO เป็นตัวแทนของกลุ่มยีนที่มีการกำหนดอย่างชัดเจน ซึ่งแตกต่างอย่างชัดเจนจากพื้นที่ราบ Tropea และ Montoro ซึ่งมักถูกเข้าใจผิด เพื่อให้คำอธิบายของกระเปาะซึ่งมักใช้สำหรับการบริโภคสด จึงมีการประเมินปริมาณของแข็งที่ละลายน้ำได้และความเผ็ด ซึ่งแสดงความหวานที่สูงขึ้นใน ARO เมื่อเทียบกับพืชสองชนิดที่กล่าวถึงข้างต้น โดยรวมแล้ว การศึกษานี้มีประโยชน์สำหรับการประเมิน ARO ในอนาคต ซึ่งสามารถส่งเสริมผ่านฉลากคุณภาพ ซึ่งอาจนำไปสู่การจำกัดการฉ้อฉลในเชิงพาณิชย์และปรับปรุงรายได้ของเกษตรกรรายย่อย
บทนำ
สกุล Allium มีประมาณ 750 สปีชีส์ [1] ซึ่งในบรรดาหัวหอม (Allium cepa L., 2n = 2x =16) เป็นหนึ่งในสกุลที่แพร่หลายที่สุด A. cepa มีวงจรทุกๆ สองปีและพฤติกรรมการสืบพันธุ์แบบผสมข้ามสายพันธุ์ ปัจจุบัน การผลิตหัวหอมทั่วโลก (97.9 Mt) ทำให้เป็นพืชผักที่สำคัญเป็นอันดับสองรองจากมะเขือเทศ [2] ตั้งแต่สมัยโบราณ หัวหอมถูกนำมาใช้ทั้งเป็นอาหารและใช้เป็นยาพื้นบ้าน แท้จริงแล้ว ชาวอียิปต์โบราณได้รายงานสูตรการรักษาหลายสูตรที่ใช้กระเทียมและหัวหอมในกระดาษปาปิรุสทางการแพทย์ของ Codex Ebers เมื่อ 1550 ปีก่อนคริสตกาล [3]
ผักอเนกประสงค์และดีต่อสุขภาพนี้บริโภคดิบ สด หรือเป็นผลิตภัณฑ์แปรรูป และใช้เพื่อเพิ่มรสชาติของอาหารหลายชนิด การศึกษาล่าสุดหลายชิ้นอ้างว่าการบริโภคหัวหอมอาจลดความเสี่ยงต่อโรคหัวใจและหลอดเลือด [4,5] โรคอ้วน [6] โรคเบาหวาน [7] และมะเร็งรูปแบบต่างๆ [8-10] คุณค่าทางโภชนาการของหัวหอมมักเกิดจากสารประกอบทางโภชนาการ XNUMX ประเภทในระดับสูง ได้แก่ ฟลาโวนอยด์และอัลค์(en)อิลซิสเทอีนซัลไฟด์ (ACSOs) ชั้นแรกประกอบด้วยฟลาโวนอลและแอนโทไซยานิน Quercetin เป็นฟลาโวนอลหลักที่ตรวจจับได้ ซึ่งเป็นที่รู้จักสำหรับสารต้านอนุมูลอิสระที่แข็งแกร่งและคุณสมบัติต้านการอักเสบในการขับอนุมูลอิสระและจับกับไอออนโลหะทรานซิชัน [11]; ในขณะที่แอนโธไซยานินให้สีแดง/ม่วงแก่หัวหอมบางพันธุ์ สำหรับ ACSOs ที่มีอยู่มากที่สุดคือ isoalliin [(+)-trans-S-1-propenyl-L-cysteine sulfoxide] [12]กรดอะมิโนกำมะถันที่ไม่ระเหยและไม่สร้างโปรตีนที่เก็บอยู่ในเซลล์ ซึ่งมีหน้าที่รับผิดชอบทางอ้อมต่อกลิ่นฉุนและรสชาติของหัวหอม [13]. เมื่อเนื้อเยื่อถูกทำลาย isoalliin จะถูกแยกออกโดยเอนไซม์ alliinase เพื่อผลิตสารประกอบระเหย (pyruvate, ammonia, thiosulphonates และ propanethial S-oxide) ซึ่งทำให้เกิดการฉีกขาดและทำให้เกิดกลิ่นไม่พึงประสงค์ (pungency) [14]. ความฉุนของหัวหอมมักจะวัดจากปริมาณต่อกรัมของน้ำหนักสดของกรดไพรูวิคที่เกิดจากการไฮโดรไลซิส [15,16].
ในประเทศลุ่มน้ำเมดิเตอร์เรเนียนเสนอเป็นหนึ่งในศูนย์ความหลากหลายรองของ A.cepa [17,18]หัวหัวหอมแสดงรูปร่าง ขนาด สี วัตถุแห้ง และความฉุนได้หลากหลาย [19-หนึ่ง]. ยิ่งไปกว่านั้น การใส่ปุ๋ยที่มีกำมะถันเป็นหลัก การปฏิบัติทางการเกษตร ชนิดของดิน สภาพภูมิอากาศ และจีโนไทป์ของพันธุ์หรือสายพันธุ์ที่ดินสามารถมีอิทธิพลต่อคุณภาพของหลอดไฟโดยการให้คุณค่าทางประสาทสัมผัสและคุณค่าทางโภชนาการที่แปลกประหลาด [23-หนึ่ง]. ในอิตาลี แม้จะมีการแพร่กระจายของหัวเชื้อหัวหอมในวงกว้าง แต่ก็มีหัวหอมเพียงไม่กี่สายพันธุ์เท่านั้นที่มักได้รับการศึกษาทางวิทยาศาสตร์และจำแนกลักษณะที่เหมาะสม [28,29].
การแสดงลักษณะทางพันธุกรรมและฟีโนไทป์อย่างละเอียดของความหลากหลายทางชีวภาพทางการเกษตรเป็นสิ่งสำคัญเพื่อให้มั่นใจว่ามีการอนุรักษ์ทรัพยากรพันธุกรรมพืชอย่างเหมาะสม และส่งเสริมการใช้ยีนเฉพาะในห่วงโซ่คุณค่า [30-หนึ่ง]. เครื่องหมาย Simple Sequence Repeat (SSR) มักถูกเลือกสำหรับการแมป [33-หนึ่ง], ลายพิมพ์ดีเอ็นเอและการเลือกปฏิบัติพันธุ์ [36-หนึ่ง]และการประมาณค่าความแปรปรวนทางพันธุกรรมที่เชื่อถือได้ภายในและระหว่างเผ่าพันธุ์ [39-หนึ่ง]เนื่องจากมีตำแหน่งเฉพาะ, หลายอัลลีล, สืบทอดโคโดมิแนนต์, ทำซ้ำได้สูง และเหมาะสำหรับการสร้างจีโนไทป์แบบอัตโนมัติ
ในการศึกษาครั้งนี้ เรามุ่งความสนใจไปที่พันธุ์พื้นเมืองของ Apulian นั่นคือ “ต้นหอมแดง Acquaviva” (ARO) ซึ่งปลูกตามวิธีการเกษตรอินทรีย์ในพื้นที่เล็กๆ ของเมือง Acquaviva delle Fonti ในจังหวัด Bari (อาพูเลีย, อิตาลีตอนใต้). หัวของพันธุ์ Landrace นี้มีขนาดใหญ่และแบนและมีสีแดง และส่วนใหญ่ใช้ในสูตรอาหารท้องถิ่น แม้ว่า ARO จะได้รับเครื่องหมายคุณภาพ "Slow Food Presidium" แต่การผลิตสามารถได้รับการส่งเสริมและปกป้องเพิ่มเติมโดยเครื่องหมายคุณภาพของสหภาพยุโรป เช่น สิ่งบ่งชี้ทางภูมิศาสตร์ที่ได้รับการคุ้มครอง (PGI) และการกำหนดแหล่งกำเนิดที่ได้รับการคุ้มครอง (POD) เนื่องจากเครื่องหมายเหล่านี้อาจมีส่วนช่วยในการจำกัด การฉ้อฉลทางการค้าและปรับปรุงรายได้ของเกษตรกรรายย่อย ในที่นี้ เครื่องหมายโมเลกุล SSR ถูกใช้เป็นเครื่องมืออันทรงพลังในการประเมินความผันแปรทางพันธุกรรมของประชากร ARO และเพื่อแยกแยะดินแดนนี้จากดินแดนต้นหอมแดงทางตอนใต้ของอิตาลีอีกสองแห่ง นอกจากนี้ เรายังประเมินความฉุนและปริมาณของแข็งที่ละลายน้ำได้เพื่อประเมินรสชาติของ ARO ที่สัมพันธ์กับความต้องการของตลาด
ผลสอบ
การจัดทำชุดรวบรวมเชื้อพันธุกรรมหัวหอมแดง Acquaviva และการศึกษาลักษณะทางสัณฐานวิทยา
เมล็ดพันธุ์ของ ARO landrace จำนวน 13 สายพันธุ์ ซึ่งบริจาคโดยเกษตรกรในกรอบของโครงการ BiodiverSO Apulia Region ถูกนำมาใช้เพื่อสร้างคอลเลกชัน ARO germplasm
ตัวบอกลักษณะทางสัณฐานวิทยาที่เกี่ยวข้องกับกระเปาะ ผิวหนัง และเนื้อถูกรวบรวมบน ARO germplasm และบนหัวหอมสามต้น โดยสองต้นเป็นของ “Tropea red onion” (TRO) landrace และอีกหนึ่งของ “Montoro copper onion” (MCO) landrace (รูปที่ 1). หลอด ARO ทั้งหมดมีลักษณะแบนและมีลักษณะพิเศษคือผิวภายนอกสีแดงและเนื้อในที่มีเฉดสีแดงต่างกัน ในทางตรงกันข้าม เนื้อของหลอด TRO มีสีแดงเต็มที่ ในขณะที่เนื้อของหลอด MCO มีเม็ดสีไม่ดี (ตารางที่ S1) การวิเคราะห์ทางชีวเคมีทำให้สามารถประเมินปริมาณของแข็งที่ละลายน้ำได้และความฉุน ดังรายงานในตาราง 1, ค่าเฉลี่ยของปริมาณของแข็งที่ละลายน้ำได้ของกระเปาะในประชากร ARO คือ 7.60 และอยู่ในช่วงตั้งแต่ 6.00 (ARO12) ถึง 9.50° Brix (ARO11 และ ARO13) ค่านี้สูงกว่าค่าที่ประมาณไว้สำหรับ TRO และ MCO landraces (4.25 และ 6.00° Brix ตามลำดับ)

1 ตาราง ปริมาณของแข็งที่ละลายน้ำได้และค่าความฉุนที่ประเมินในประชากร “Acquaviva Red Onion” (ARO), “Tropea Red Onion” (TRO) และ “Montoro Copper Onion” (MCO) *
| รหัส | ปริมาณของแข็งที่ละลายน้ำได้ (Brix) | ความฉุน (pมล-1 เอฟดับบลิว) | ||
| หมายความ | CV y (%) | หมายความ | CV y (%) | |
| ARO1 | 6.25 วัน * | 5.65 | 5.84 เอบี * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 | 22.98 |
| ARO3 | 7.50 ปีก่อนคริสตกาล | 9.42 | 5.28 อะบี | 22.88 |
| ARO4 | 7.50 ปีก่อนคริสตกาล | 0.00 | 6.97 | 3.74 |
| HOOP 5 | 7.50 ปีก่อนคริสตกาล | 0.00 | 6.80 | 9.68 |
| ARO6 | D 6.25 | 5.65 | 4.51 อะบี | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 อะบี | 15.44 |
| ARO8 | AB 9.00 | 0.00 | 7.04 | 3.49 |
| ARO9 | 8.25 เอบีซี | 4.28 | 6.84 | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 อะบี | 6.57 |
| ARO11 | 9.50 | 7.44 | 5.54 อะบี | 16.43 |
| ARO12 | D 6.00 | 0.00 | 4.91 อะบี | 9.70 |
| ARO13 | 9.50 | 7.44 | 6.63 | 24.93 |
| MCO | D 6.00 | 0.00 | 4.18 อะบี | 2.66 |
| โทร1 | E 4.25 | 8.31 | 2.80 ข | 2.10 |
| โทร2 | E 4.25 | 8.31 | 4.28 อะบี | 4.79 |
* ค่าเฉลี่ยที่มีตัวอักษรเดียวกันเป็นตัวพิมพ์ใหญ่หรือตัวพิมพ์เล็กไม่มีความแตกต่างทางสถิติที่ 0.01P หรือ 0.05P ตามลำดับ (การทดสอบของ SNK) y ค่าสัมประสิทธิ์การแปรผัน
ค่าเฉลี่ยของความฉุน ARO ซึ่งประเมินโดยวิธีปริมาณกรดไพรูวิกคือ 6.00 ซึ่งอยู่ในช่วง 4.51 pmol g-1 FW (ARO6) ถึง 7.04 (ARO8) ค่านี้สูงกว่าค่าที่ประมาณได้ใน TRO และ MCO landraces (3.54 pmol g-1 FW และ 4.18 น. ก-1 FW ตามลำดับ).
SSR Polymorphism และความสัมพันธ์ทางพันธุกรรมระหว่างภาคยานุวัติ
ในการศึกษาปัจจุบัน 11 จาก 37 ชุดค่าผสมไพรเมอร์ SSR ที่ทดสอบให้ความหลากหลายแบบโลคัสเดียว กล่าวคือ ให้ผลผลิตสูงสุดสองผลิตภัณฑ์ในหนึ่งเดียว โดยรวมแล้ว ตรวจพบอัลลีล 55 รายการในบุคคล 320 คนโดยมีจำนวนอัลลีลต่อโลคัสตั้งแต่ 2 (ACM147 และ ACM 504) ถึง 11 (ACM132) และค่าเฉลี่ย 5 อัลลีล (ตาราง 2). ในแต่ละประชากร จำนวนอัลลีล (Na) อยู่ในช่วงตั้งแต่ 1.94 (ACM147 และ ACM504) ถึง 5.38 (ACM132) ในขณะที่จำนวนอัลลีล (Ne) ที่มีประสิทธิผลอยู่ในช่วงตั้งแต่ 1.41 (ACM152) ถึง 2.82 (ACM449) ความแตกต่าง ระหว่างค่า Na และ Ne เกิดจากการมีอัลลีลที่มีความถี่ต่ำในประชากรและอัลลีลเด่นเพียงไม่กี่ตัว ค่า heterozygosity (Ho) ที่สังเกตได้สูงสุดถูกเน้นสำหรับ ACM138 และ ACM449 (0.62) ในขณะที่ค่าต่ำสุดนั้นสัมพันธ์กับ ACM152 (0.25) ภาวะ heterozygosity ที่คาดหวัง (He) ซึ่งสอดคล้องกับความคาดหวังทางทฤษฎีในกลุ่มประชากรที่มีการระบาดใหญ่ มีค่าตั้งแต่ 0.37 (ACM504) ถึง 0.61 (ACM132, ACM138 และ ACM449) ดัชนีการตรึงของไรท์ (Fis) แสดงค่าใกล้ศูนย์ (ค่าเฉลี่ย 0.05) สำหรับเครื่องหมายทั้งหมด โดยระบุค่าที่คล้ายคลึงกันระหว่างระดับ heterozygosity ที่สังเกตได้และที่คาดไว้ ตามที่คาดไว้สำหรับสปีชีส์ที่ผสมข้ามสายพันธุ์ ประสิทธิภาพของเครื่องหมาย SSR แต่ละตัวในการตรวจลายนิ้วมือทางพันธุกรรมถูกประเมินโดยดัชนีเนื้อหาข้อมูลโพลีมอร์ฟิค (PIC) โดยมีค่าเฉลี่ย 0.48 และอยู่ในช่วงตั้งแต่ 0.33 (ACM504) ถึง 0.67 (ACM132) ดัชนีประสิทธิภาพอีกดัชนีหนึ่งคือ Shannon's Information Index (I) แสดงค่าเฉลี่ยที่ 0.84 และค่าที่สมมติขึ้นอยู่ในช่วงตั้งแต่ 0.45 (ACM152) ถึง 1.20 (ACM132)
2 ตาราง คุณสมบัติความแตกต่างของเครื่องหมาย SSR 11 ตัวที่ใช้ในการประเมินความหลากหลายทางพันธุกรรมในประชากร ARO, TRO และ MCO จำนวนรวมของอัลลีล (Na) ช่วงขนาดแถบ และดัชนีเนื้อหาข้อมูลโพลีมอร์ฟิค (PIC) อ้างถึงชุดรวมของบุคคล 320 จีโนไทป์ในการศึกษานี้ จำนวนอัลลีล (Na), จำนวนอัลลีลที่มีประสิทธิผล (Ne), ความแตกต่างที่สังเกตได้ (Ho), ความแตกต่างที่คาดหวัง (He), ดัชนีการตรึง (Fis) และดัชนีข้อมูลของแชนนอน (I) หมายถึงค่าเฉลี่ยที่คำนวณจากประชากร 16 คน แต่ละกลุ่มประกอบด้วยบุคคล 20 คน
| โลกัส. | รวมนา | ช่วงขนาด (bp) | PIC | หมายความ | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| หมายความ | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
ในบรรดาประชากร ARO3, ARO6, ARO8, ARO10, TRO1 และ MCO แสดงการแปรผันทางพันธุกรรมในระดับสูง (Ho > 0.5) ในขณะที่ความหลากหลายต่ำที่สุดถูกสังเกตพบในประชากร ARO7 (Ho = 0.27) (ตารางเสริม S2) โดยรวมแล้ว ภาคยานุวัติทั้งหมดที่แสดง Fis ค่าใกล้ศูนย์ (Fis ค่าเฉลี่ย = 0.054) ตามที่คาดไว้ภายใต้เงื่อนไขการผสมพันธุ์แบบสุ่ม
การวิเคราะห์ความแปรปรวนของโมเลกุลและโครงสร้างทางพันธุกรรม
การแบ่งลำดับชั้นของความแปรปรวนทางพันธุกรรมระหว่างและภายในประชากรถูกคำนวณโดย AMOVA ผลการวิจัยเน้นความแปรผันทางพันธุกรรมในประชากร (87%) ความแตกต่างระหว่างประชากร 13% มีนัยสำคัญอย่างมาก (P < 0.001) (ตาราง 3). ค่าแบบคู่ของพารามิเตอร์ Fpt ซึ่งเป็นค่าอะนาล็อกของดัชนีการตรึง Fst ของไรท์ ซึ่งมีค่าตั้งแต่ 0.002 (ARO2/ARO10) ถึง 0.468 (ARO7/TRO2) มีนัยสำคัญ (P < 0.05) ยกเว้นการเปรียบเทียบเก้าคู่ (ตารางเสริม S3)
3 ตาราง การวิเคราะห์ความแปรปรวนของโมเลกุลของ 320 จีโนไทป์จาก 16 ประชากรของ Allium cepa L.
| แหล่ง | df | ผลรวมของสี่เหลี่ยม | การประมาณค่าความแปรปรวน | ความแปรปรวน (%) | Fpt | P |
| ในหมู่ประชากร | 15 | 458.63 | 1.16 | 13% | ||
| ภายในกลุ่มประชากร | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| รวม | 319 | 2731.62 | 8.66 |
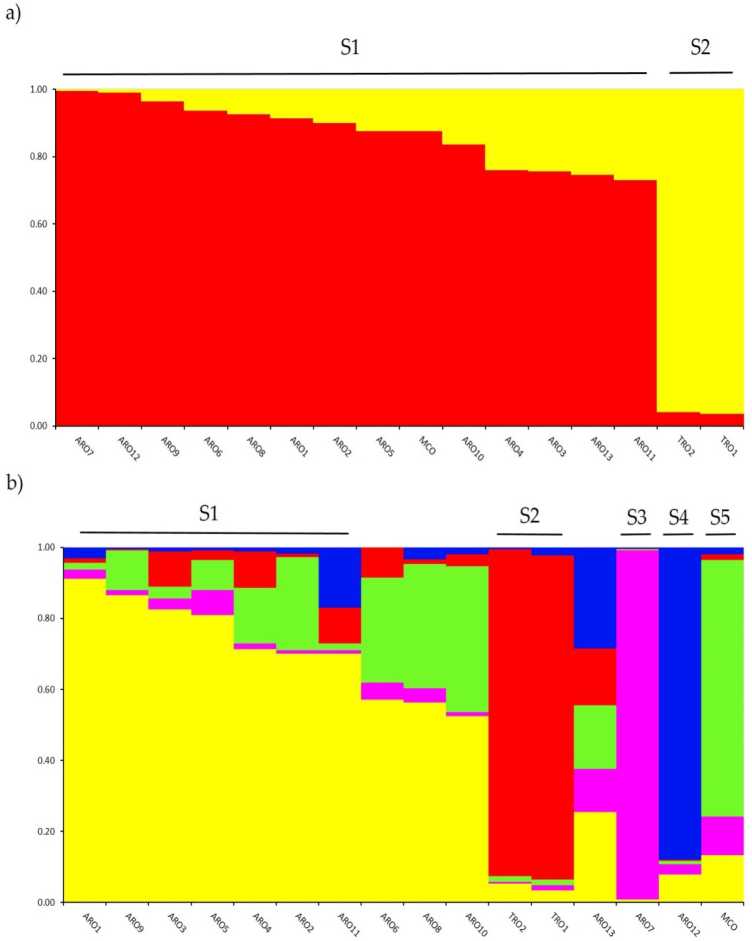
การตรวจสอบโครงสร้างทางพันธุกรรมใน A.cepa การรวบรวมจีโนไทป์ในการศึกษานี้ดำเนินการโดยการวิเคราะห์การจัดกลุ่มตามแบบจำลองของส่วนผสมที่ใช้ในโครงสร้างซอฟต์แวร์ วิธี Evanno AK แนะนำให้แบ่งกลุ่มออกเป็นสองกลุ่ม (K = 2) ซึ่งเป็นข้อมูลที่ดีที่สุดสำหรับเรา ชุด,กับ the ถัดไป pe สูงสุดak ที่ K = 5 (อาหารเสริม Rgure เอส1). สำหรับ K = 2, aแรงม้าopระเบียบวเป็นตูดigned ด้วยnof ทั้งสองกลุ่ม กับ ค่าสัมประสิทธิ์ rnernbertoip (q) > 0.7 ในฐานะที่เป็นhoชนะใน รูป 2aคลัสเตอร์แรก (ชื่อ S1) รวม MCO และประชากร ARO ทั้งหมด ในขณะที่คลัสเตอร์ S2 จัดกลุ่มประชากร TRO สองตัว ที่ K = 5 ให้คำอธิบายที่ลึกกว่าของชุดข้อมูล (รูปที่ 2b) 75% ของการเข้าใช้ถูกกำหนดให้กับหนึ่งในห้าคลัสเตอร์ การแยกระหว่าง ARO (S1) และ TRO (S2) ได้รับการยืนยัน แม้ว่าประชากร ARO บางส่วนจะถูกผสม (q < 0.7) หรือจัดกลุ่มแยกกันในสองกลุ่มใหม่ S3 และ S4 (ARO7 และ ARO12 ตามลำดับ) ที่น่าสนใจคือ MCO ประเภทการค้าสร้างกลุ่มที่แตกต่างกัน (S5) แยกจากหอมแดง Apulian
ความสัมพันธ์ทางพันธุกรรมระหว่างประชากร
ความหลากหลายของ SSR อนุญาตให้วาด dendrogram ของความหลากหลายทางพันธุกรรมและผลลัพธ์ของการวิเคราะห์สายวิวัฒนาการจะแสดงในรูป 3a. ที่นี่ คอลเลกชันของเชื้อโรคถูกแบ่งออกเป็นห้ากลุ่มซึ่งได้รับการสนับสนุนอย่างมากจากค่าบูทสแตรป ประชากร ARO7 และ ARO12 ถูกแยกออกจากประชากรที่เหลือทันทีและก่อตัวเป็นสองกลุ่มที่แตกต่างกัน คลัสเตอร์ที่สามประกอบด้วยประชากรเชิงพาณิชย์สองตัวของ TRO ในขณะที่โหนดที่สี่แบ่ง MCO จากประชากร ARO สิบเอ็ดตัว ความสัมพันธ์ทางพันธุกรรมที่เกิดขึ้นในหมู่ประชากรถูกตรวจสอบเพิ่มเติมโดยการวิเคราะห์พิกัดหลัก (PCoA) (รูปที่ 3b). ตามที่เน้นไว้ก่อนหน้านี้ ประชากร ARO ถูกจัดกลุ่มอย่างแน่นหนา ยกเว้น ARO12 และ ARO7 ซึ่งปรากฏในตำแหน่งแยกในแผนภาพ PCoA TRO สองตัวและประชากร MCO กระจายอยู่ในแผงด้านขวาล่างของโครงเรื่อง
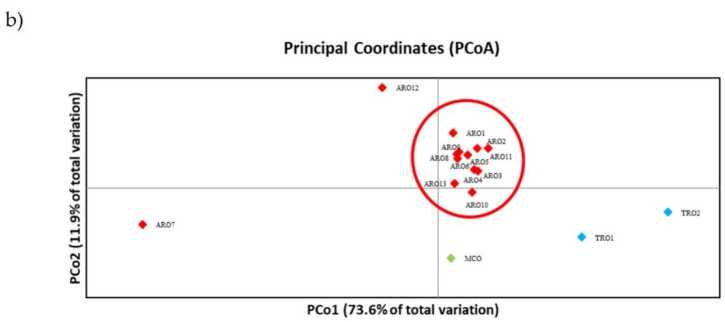
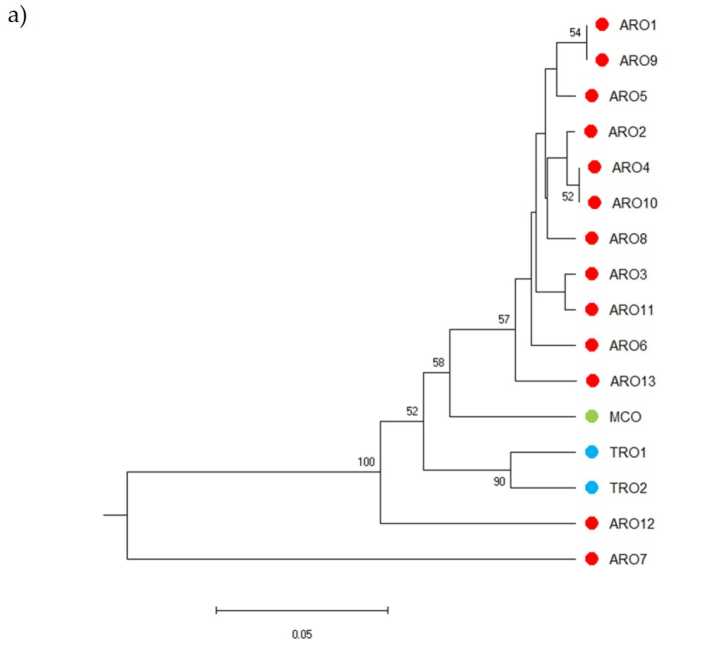
รูป 3 ความหลากหลายทางพันธุกรรมหมู่ที่ 16 A.cepa ประชากรที่มีลักษณะเฉพาะในการศึกษานี้ ตามโปรไฟล์ SSR ของพวกเขา (a) UPGMA dendrogram ของระยะพันธุกรรม. ค่าสนับสนุน Bootstrap >50 ถูกระบุเหนือโหนดที่เกี่ยวข้อง (b) การวิเคราะห์องค์ประกอบหลัก (PCoA) คลัสเตอร์ที่วงกลมด้วยสีแดงเข้าคู่กับกลุ่มที่สร้างขึ้นโดยการวิเคราะห์สายวิวัฒนาการและประกอบขึ้นด้วยการเข้าถึง ARO 11 รายการ
การสนทนา
ภายในความหลากหลายทางชีวภาพทางการเกษตรจำนวนมากที่ปลูกแบบดั้งเดิมในภาคใต้ของอิตาลี พื้นที่ปลูกหัวหอมเป็นตัวแทนของผลิตภัณฑ์เฉพาะกลุ่มที่จำเป็นต้องรักษาไว้จากความเสี่ยงของการสึกกร่อนของพันธุกรรมและการคุกคามของการแทนที่โดยพันธุ์สมัยใหม่ ในกรอบของโครงการระดับภูมิภาค BiodiverSO ซึ่งมุ่งเป้าไปที่การรวบรวม ระบุลักษณะ ส่งเสริม และปกป้องทรัพยากรพันธุกรรมของภูมิภาค Apulia ที่เชื่อมโยงอย่างมากกับมรดกท้องถิ่น เราได้จัดตั้งกลุ่มประชากร 13 สายพันธุ์ของ ARO landrace เรารายงานการประเมินครั้งแรกของการแปรผัน ARO ในแง่ของความหลากหลายทางดีเอ็นเอและพารามิเตอร์ทางชีวเคมีสองค่า ของแข็งที่ละลายน้ำได้และปริมาณกรดไพรูวิค ที่เกี่ยวข้องกับลักษณะรสชาติและความสำคัญสำหรับการยอมรับผลิตภัณฑ์สดที่ยังไม่ได้ปรุง นอกจากนี้ ข้อมูลเกี่ยวกับ ARO landrace ถูกนำไปเปรียบเทียบกับข้อมูลที่รวบรวมบน landraces หัวหอมที่มีเม็ดสีอีกสองชนิดซึ่งมักจะเข้าใจผิด
การวิเคราะห์ทางชีวเคมีเน้นที่ความหวานของประชากร ARO 13 ชนิด ซึ่งเกี่ยวข้องกับปริมาณของแข็งที่ละลายน้ำได้สูงและความฉุนปานกลาง ตามแนวทางของอุตสาหกรรมหัวหอมหวาน [31]. หลอด ARO มีความหวานมากกว่าหลอด TRO และ MCO และมีความฉุนสูงกว่าเล็กน้อย อย่างไรก็ตาม ความหวานในหัวหอมเกิดจากความสมดุลระหว่างปริมาณน้ำตาลและความฉุน ดังนั้น การแสดงลักษณะนี้จึงมีประโยชน์ในการสนับสนุนการเลือกจีโนไทป์ของมูลค่า ซึ่งมักจะดำเนินการโดยเกษตรกรโดยพิจารณาจากลักษณะทางสัณฐานวิทยาเท่านั้น
เครื่องหมาย SSR ได้รับการยืนยันว่าเป็นเครื่องมือที่มีประโยชน์ในการแยกแยะจีโนไทป์ แม้ว่าจะถูกรวบรวมในพื้นที่เติบโตแคบๆ เช่น เมืองอักควาวิวา เดลเล ฟอนติ เครื่องหมายที่เลือกแสดงจำนวนอัลลีลที่สูงกว่าเครื่องหมายที่รายงานไว้ก่อนหน้านี้ [43] และ [44]แต่ต่ำกว่าเครื่องหมายที่รายงานโดย [45]. นอกจากนี้ 50% ของชุดเครื่องหมายของเราแสดงค่าดัชนี PIC มากกว่า 0.5 ซึ่งพิสูจน์ได้ว่าเหมาะสมในการแยกแยะกลุ่มประชากรในคอลเล็กชันตามคำแนะนำของ [46]. การประเมินความหลากหลายภายในประชากรเผยให้เห็นค่าที่คล้ายคลึงกันระหว่าง Ho และ He ส่งผลให้ Fi ต่ำs ค่า สิ่งนี้สอดคล้องกับลักษณะการข้ามของ ก. เซปา ซึ่งป่วยหนักจากโรคซึมเศร้าทางสายเลือด [47]. Fi โดยรวมs ค่าที่คำนวณในประชากรหัวหอมที่พิจารณาในการศึกษานี้ (0.054) ต่ำกว่าค่าที่รายงานไว้ก่อนหน้านี้ [45] (0.22) และเกือบจะเหมือนกับที่พบโดย [31] (0.08) และ [48] (0.00) ที่ประเมินความหลากหลายทางพันธุกรรมในดินแดนหัวหอมจากทางตะวันตกเฉียงเหนือของสเปนและไนเจอร์ ตามลำดับ ระดับ heterozygosity ที่น่าสังเกตในประชากร ARO ช่วยเสริมแนวคิดที่ว่า Apulia เป็นตัวแทนของศูนย์ความหลากหลายสำหรับพืชสวนหลายชนิด [32, 42, 49-หนึ่ง].
AMOVA เน้นว่าการแปรผันของโมเลกุลส่วนใหญ่ในคอลเล็กชันจีโนไทป์ในการศึกษานี้อยู่ในกลุ่มประชากร อย่างไรก็ตาม ความแตกต่างทางพันธุกรรมระหว่างกลุ่มประชากร (FPT ค่า) เปิดเผยการเกิดการแบ่งชั้นทางพันธุกรรม ในความเป็นจริง แม้ว่าผลลัพธ์ของเราจะบ่งชี้ว่ามีความสม่ำเสมอทางพันธุกรรมในประชากร ARO ส่วนใหญ่ ซึ่งก่อตัวเป็นคลัสเตอร์ที่ชัดเจน แต่ประชากร ARO7 และ ARO12 ก็แสดงโปรไฟล์ทางพันธุกรรมที่แตกต่างกันอย่างชัดเจน ผลลัพธ์นี้อาจเกิดจากแหล่งที่มาที่แตกต่างกันของเมล็ดพันธุ์ที่ใช้โดยเกษตรกรสองรายที่รวบรวมประชากร ยิ่งไปกว่านั้น จากผลลัพธ์ที่ได้ ARO landrace สามารถพิจารณาได้อย่างชัดเจนในระดับพันธุกรรมจาก TRO และ MCO landrace ในการศึกษาล่าสุดพบว่า [29] ประเมินความหลากหลายทางพันธุกรรมของหัวหอมในอิตาลีหลายสายพันธุ์ รวมถึง “Acquaviva” “Tropea” และ “Montoro” แม้ว่าผู้เขียนจะใช้เครื่องหมาย SNP เพื่อประเมินความหลากหลายทางพันธุกรรมของคอลเลกชันหัวหอมที่กว้างขึ้น แต่การสร้างจีโนไทป์ไม่สามารถแยกแยะ "Acquaviva" จาก "Tropea" และ "Montoro" หัวหอมได้ อาจเป็นไปได้ว่าความคลาดเคลื่อนนี้เกิดจากค่า PIC เฉลี่ยต่ำที่พบ (0.292) ซึ่งบ่งชี้ถึงข้อมูลทั่วไปที่พอประมาณของตำแหน่งภายใต้การวิเคราะห์ตามที่อ้างโดย [29]. นอกจากนี้ เพื่อที่จะตรวจสอบการมีอยู่ของโครงสร้างย่อยในคลัสเตอร์อิตาลี จะเป็นการดีกว่าหากวิเคราะห์จีโนไทป์ของอิตาลีแยกต่างหากจากคอลเล็กชันที่เหลือ อาจเป็นไปได้ที่จะทำให้เห็นภาพรูปแบบของความหลากหลายทางพันธุกรรมที่เชื่อมโยงกับการแบ่งชั้นทางภูมิศาสตร์หรือลักษณะเฉพาะภายใต้การเลือกเชิงประจักษ์
โดยสรุป การศึกษานี้นำเสนอรายงานที่ครอบคลุมเกี่ยวกับพื้นที่ปลูกหัวหอมที่เกี่ยวข้องกับมรดกทางวัฒนธรรมท้องถิ่นและมีความสำคัญทางเศรษฐกิจสำหรับเกษตรกร ผลลัพธ์ของเราเน้นว่ามีข้อยกเว้นบางประการ ARO มีลักษณะเฉพาะของยีนพูลที่ชัดเจน ซึ่งสมควรได้รับการอนุรักษ์จากความเสี่ยงของการพังทลายของยีน ดังนั้นการจัดตั้งกลุ่มตัวแทนของแหล่งความหลากหลายทางพันธุกรรมอันมีค่านี้จึงมีความสำคัญอย่างยิ่ง ประการสุดท้าย ลักษณะทางพันธุกรรมและฟีโนไทป์ของ ARO อาจเป็นประโยชน์ในการได้รับเครื่องหมายคุณภาพจากสหภาพยุโรป
วัสดุและวิธีการ
การรวบรวมเชื้อจุลินทรีย์ วัสดุจากพืช และการสกัดดีเอ็นเอ
ประชากร 13 ชุดของ ARO landrace ได้มาภายใต้กรอบของโครงการ Apulia Region (BiodiverSO: https://www.biodiversitapuglia.it/)ผ่านชุดของภารกิจที่ดำเนินการใน "Acquaviva delle Fonti" เมือง Apulian ขนาดเล็กในจังหวัด Bari ประเทศอิตาลี ไซต์รวบรวมของแต่ละภาคยานุวัติถูกแมปผ่านระบบสารสนเทศภูมิศาสตร์ (GIS) และรายงานในตาราง 4. นอกจากนี้ ประชากรสองคนจาก TRO landrace และหนึ่งประชากรจาก MCO landrace ถูกรวมไว้ในการศึกษานี้และใช้เป็นข้อมูลอ้างอิง วัสดุจากพืชทั้งหมดปลูกในสภาพแวดล้อมเดียวกันที่ฟาร์มทดลอง “P Martucci” ของมหาวิทยาลัย Bari (41° 1'22.08″ N, 16°54'25.95″ E) ภายใต้กรงป้องกันเพื่อหลีกเลี่ยงการผสมเกสรข้ามหมู่ ประชากรและการผสมเกสรภายในประชากรโดยแมลงวัน (ลูซิเลีย ซีซาร์). ประชากร 16 คนมีลักษณะเฉพาะที่เกี่ยวข้องกับขนาดและรูปร่างของกระเปาะ และผิวหนังและสีเนื้อ (ตารางที่ S1) นอกจากนี้ การทดสอบปริมาณของแข็งที่ละลายน้ำได้ดำเนินการโดยใช้เครื่องวัดการหักเหของแสงแบบมือถือ และวัดความเผ็ดร้อนในตัวอย่างน้ำหัวหอมที่เติม 2,4-ไดไนโทรฟีนิล ไฮดราซีน (0.125% v/v ใน 2N ของ HCl) และประเมินค่าการดูดกลืนแสงที่ 420 นาโนเมตร ตามที่รายงานโดย [31]. การทดสอบแบบหลายช่วงของ Duncan และการทดสอบ SNK ดำเนินการเพื่อระบุความแตกต่างที่มีนัยสำคัญ
4 ตาราง รายชื่อประชากรที่รวบรวมและจีโนไทป์ในการศึกษานี้ สำหรับแต่ละประชากร รหัสประจำตัว ชื่อท้องถิ่น พิกัด GPS และ Gene Bank Preserving the Seeds จะถูกรายงาน
| รหัส | Name | พิกัด GPS | ธนาคารยีน y |
| ARO1 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°54’21.708″ N 16°49’1.631” E | ศอ.บต |
| ARO2 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°53’14.28″ N 16°48’56.879” E | ศอ.บต |
| ARO3 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°54’11.304″ N 16°49’13.079” E | ศอ.บต |
| ARO4 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°54’3.348″ N 16°40’27.011” E | ศอ.บต |
| ARO5 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°51’59.76″ N 16°53’0.527” E | ศอ.บต |
| ARO6 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°52’48.72″ N 16°49’43.247” E | ศอ.บต |
| ARO7 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°53’13.47″ N 16°50’23.783” E | ศอ.บต |
| ARO8 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°53’18.816″ N 16°49’33.888” E | ศอ.บต |
| ARO9 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°54'51.372″ น 16°49'3.504" E | ศอ.บต |
| ARO10 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°54’1.188″ N 16°49’24.311” E | ศอ.บต |
| ARO11 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°52'49.8″ น 16°49'48.575" E | ศอ.บต |
| ARO12 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°52’38.892″ N 16°49’28.379” E | ศอ.บต |
| ARO13 | ซิโปลลา รอสซา ดิ อควาวีวา | 40°53’21.768″ N 16°49’29.711” E | ศอ.บต |
| โทร1 | Cipolla rossa lunga di Tropea | - | ศอ.บต |
| โทร2 | ชิโปลลา รอสซา ทอนดา ดิ โตรเปีย | - | ศอ.บต |
| MCO | ซิโปลลา รามาตา ดิ มอนโทโร | - | ศอ.บต |
| y Di.SSPA ภาควิชาวิทยาศาสตร์ดิน พืช และอาหาร มหาวิทยาลัยบารี |
เก็บตัวอย่างวัสดุจากใบไม้ 20 จีโนไทป์ต่อประชากรและเก็บไว้ที่ -80 °C จนกว่าจะใช้งาน สำหรับสายพันธุ์ที่อุดมด้วยโพลีแซคคาไรด์ เช่น ก. เซปา ขั้นตอนแรก การกำจัดพอลิแซ็กคาไรด์เป็นสิ่งจำเป็นเพื่อให้ได้ DNA ที่มีคุณภาพ ดังนั้นการล้างครั้งแรกในบัฟเฟอร์ STE (0.25 M sucrose, 0.03 M Tris, 0.05 M EDTA) ได้ดำเนินการตามที่อธิบายโดย [52]. DNA ทั้งหมดถูกสกัดโดยวิธี CTAB [53] และสุดท้ายได้รับการตรวจสอบคุณภาพและความเข้มข้นด้วยเครื่องสเปกโตรโฟโตมิเตอร์ UV-vis ของ Nano Drop 2000 (ThermoScientific, Waltham, MA, USA) และ 0.8% agarose gel electrophoresis
การวิเคราะห์ SSR
ไพรเมอร์ผสม EST-SSR 16 ชนิดที่พัฒนาโดย [54] และเคยผ่านการทดสอบในการศึกษาความหลากหลายทางพันธุกรรมโดย [43] และ [44] และ SSR จีโนม 21 ตัว [45-หนึ่ง] ได้รับการคัดเลือกเพื่อประเมินความเหมาะสม (ตารางเสริม S4) จีโนไทป์ดำเนินการโดยใช้วิธีการติดแท็กเรืองแสงทางเศรษฐกิจซึ่งเพิ่มหาง M13 ลงในไพรเมอร์ SSR ไปข้างหน้าแต่ละตัว [56]. PCR ผสมถูกเตรียมในปฏิกิริยา 20 gL ที่มี: 50 ng ของ DNA ทั้งหมด, 0.2 mM ของ dNTP ผสม, 1X ของ PCR บัฟเฟอร์ปฏิกิริยา, 0.8 U ของ DreamTaq DNA polymerase (Thermo Scientific, Waltham, MA, USA), 0.16 gM ของไพรเมอร์ย้อนกลับ , 0.032 gM ของไพรเมอร์ไปข้างหน้าขยายด้วยลำดับ M13 (5′-TGTAAAACGACGCCAGT-3 ′) และ 0.08 gM ของไพรเมอร์ M13 สากลที่ติดฉลากด้วยสีย้อมเรืองแสง FAM หรือ NED (Sigma-Aldrich, St. Louis, MO, USA) ปฏิกิริยา PCR ดำเนินการในเทอร์โมไซเคิลของ SimpliAmp (Applied Biosystems, CA, USA) โดยมีเงื่อนไขต่อไปนี้สำหรับคู่ไพรเมอร์ส่วนใหญ่: 94 °C เป็นเวลา 5 นาที, 40 รอบที่ 94 °C เป็นเวลา 30 วินาที, 58 °C เป็นเวลา 45 วินาที และ 72 °C เป็นเวลา 45 วินาที และยืดตัวครั้งสุดท้ายที่อุณหภูมิ 72 °C เป็นเวลา 5 นาที สำหรับ ACM446 และ ACM449 นั้น PCR ทัชดาวน์ถูกนำมาใช้กับการหลอม 60 °C ถึง 55 °C มากกว่า 10 รอบ 30 รอบที่ 55 °C ตามด้วยการยืดเวลาสุดท้าย 5 นาทีที่ 72 °C ผลิตภัณฑ์ PCR ถูกโหลดลงในจาน 96 หลุมและผสมกับ Hi-Di Formamide (Life Technologies, Carlsbad, CA, USA) 14 gL และ GeneScan 0.5 ROX Size Standard 500 gL (Life Technologies, Carlsbad, CA, USA) แอมพลิคอนได้รับการแก้ไขโดยใช้ ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA) เครื่องหาลำดับของเส้นเลือดฝอย โดยที่อัลลีลถูกให้คะแนนเป็นโคเด่นร่วมและกำหนดโดยใช้ซอฟต์แวร์ GeneMapper เวอร์ชัน 3.7
ซอฟต์แวร์ GenAlEx 6.5 [57] และ Cervus 3.0.7 [58] ใช้ในการประมาณจำนวนอัลลีล (Na) จำนวนอัลลีลที่มีประสิทธิผล (Ne) เฮเทอโรไซโกสิตีที่สังเกตได้ (Ho) เฮเทอโรไซโกสิตีที่คาดหวัง (He) เนื้อหาข้อมูลโพลีมอร์ฟิค (PIC) ดัชนีข้อมูลแชนนอน (I) และดัชนีการตรึง (Fis ) สำหรับแต่ละโลคัส SSR
การประเมินความหลากหลายทางพันธุกรรม
การแบ่งลำดับชั้นของความแปรปรวนทางพันธุกรรมระหว่างและภายในประชากรหัวหอมได้รับการประเมินโดย GenAlEx 6.5 [57] ผ่านการวิเคราะห์ความแปรปรวนของโมเลกุล (AMOVA) ด้วย 999 bootstrapping เพื่อทดสอบนัยสำคัญ นอกจากนี้ ซอฟต์แวร์ GenAlEx 6.5 ยังใช้ประเมินความหลากหลายภายในประชากรแต่ละกลุ่มโดยคำนวณค่าเฉลี่ยของ Ho, He และ Fis จากตำแหน่ง SSR ทั้งหมด
โครงสร้างประชากรได้รับการสรุปโดยอัลกอริทึมการจัดกลุ่มตามแบบจำลอง Bayesian ที่นำมาใช้ในซอฟต์แวร์ STRUCTURE v.2.3.4 [59]. ชุดข้อมูลถูกเรียกใช้ด้วยกลุ่มสมมุติฐาน (K) จำนวนหนึ่งตั้งแต่ 1 ถึง 10 โดยตั้งค่าการทำงานอิสระ 100,000 รายการต่อค่า K แต่ละค่า สำหรับการเรียกใช้แต่ละครั้ง มีเป้าหมายเพื่อตรวจสอบความสอดคล้องของผลลัพธ์ ระยะเวลาการเบิร์นอินเริ่มต้น 100,000 ครั้ง และการวนซ้ำของ Markov Chain Monte Carlo (MCMC) XNUMX ครั้งภายใต้แบบจำลองสารผสมและความถี่อัลลีลอิสระในหมู่ประชากร ค่า K ที่เป็นไปได้มากที่สุดถูกกำหนดโดยใช้วิธี AK ซึ่งอธิบายโดย [60]ในโปรแกรมบนเว็บ STRUCTURE HARVESTER [61]. ประชากรแต่ละกลุ่มถูกกำหนดให้กับคลัสเตอร์เฉพาะเมื่อค่าสัมประสิทธิ์การเป็นสมาชิก (ค่า q) สูงกว่า 0.7 มิฉะนั้นจะถือว่ามีบรรพบุรุษแบบผสม
การวิเคราะห์พิกัดหลักดำเนินการเพื่อให้เห็นภาพรูปแบบของความสัมพันธ์ทางพันธุกรรมระหว่างภาคยานุวัติที่เปิดเผยโดยเมทริกซ์ระยะทางทางพันธุกรรมของ Nei (ตารางเสริม S5) ตามความถี่ของอัลลีล dendrogram ของระยะทางทางพันธุกรรมถูกสร้างขึ้นโดยใช้วิธีการจัดกลุ่มคู่ที่ไม่ได้ถ่วงน้ำหนักด้วยการวิเคราะห์คลัสเตอร์ค่าเฉลี่ยเลขคณิต (UPGMA) ในซอฟต์แวร์ POPTREEW [62]. Bootstrapping ถูกนำมาใช้เพื่อประเมินความเชื่อมั่นในการจัดกลุ่มแบบลำดับชั้น โดยตั้งค่าการสุ่มใหม่ 100 ชุดของชุดข้อมูล ในที่สุดซอฟต์แวร์ MEGA X [63] ถูกใช้เป็นซอฟต์แวร์วาดภาพต้นไม้
วัสดุเสริม: ออนไลน์มีให้ที่ http://www.mdpi.com/2223-7747/9/2/260/s1. ตาราง S1: ลักษณะทางสัณฐานวิทยาของหลอด ARO, MCO และ TRO ตารางที่ S2: ดัชนี heterozygosity และตรึงที่คำนวณสำหรับ ARO landraces และ TRO และ MCO landraces ตารางที่ S3: ค่าแบบคู่ของพารามิเตอร์ Fpt ตารางที่ S4: รายชื่อ SSR ที่ใช้ในการศึกษา ตาราง S5 เมทริกซ์ประชากรแบบคู่ของระยะพันธุกรรม Nei รูปที่ S1: แผนภูมิเส้นของค่า K ที่เปลี่ยนแปลงด้วย Delta K ของ Evanno
ผลงานผู้แต่ง: CL และ LR เป็นผู้คิดค้นการศึกษาและออกแบบการทดลอง CL และ PI ทำการวิเคราะห์เครื่องหมายโมเลกุล ARM และ VZ ทำการทดลองภาคสนาม RM, SP, GR และ CL มีส่วนร่วมในการวิเคราะห์ข้อมูล RM และ CL เขียนต้นฉบับ ผู้เขียนทุกคนได้อ่านและยอมรับต้นฉบับฉบับที่จัดพิมพ์แล้ว
เงินทุน: งานนี้ได้รับทุนจากโครงการ Apulian ประจำภูมิภาค “ความหลากหลายทางชีวภาพของสายพันธุ์ผัก Apulian”—Programma di Sviluppo Rurale per la Puglia 2014-2020 มิซูระ 10—ซอตโตมิซูระ 10.2; ให้ถ้วย H92C15000270002 ประเทศอิตาลี
ขอขอบคุณ: กิตติกรรมประกาศเป็นเพราะ “Azienda Agricola Iannone Anna” และ “Associazione produttori della vera cipolla rossa di Acquaviva” สำหรับการจัดหาวัสดุจากพืชที่ใช้ในการทดลอง
ความขัดแย้งที่น่าสนใจ: ผู้เขียนรายงานว่าไม่มีความขัดแย้งทางผลประโยชน์
อ้างอิง
- 1. Stearn, WT Allium รู้จักกี่ชนิด? คิวแม็ก. 1992, 9, 180-182 [CrossRef]
- 2. ฟาสแตท ฐานข้อมูลสถิติของ FAO มีจำหน่ายทางออนไลน์: http://www.fao.org/2017 (เข้าถึงเมื่อ 8 มกราคม 2019).
- 3. บล็อก, E. เคมีของกระเทียมและหัวหอม. วิทย์ am 1985, 252, 114-119 [CrossRef]
- 4. ลี บี; จุง, JH; Kim, HS การประเมินหัวหอมแดงต่อฤทธิ์ต้านอนุมูลอิสระในหนู เคมีอาหาร. สารพิษ 2012, 50, 3912 3919- [CrossRef]
- 5. ลี SM; มูน, เจ; จุง, JH; ชา, วายเจ; Shin, MJ ผลของสารสกัดจากเปลือกหัวหอมที่อุดมด้วยเควอซิทินต่อการเกิดลิ่มเลือดในหลอดเลือดแดงในหนูแรท เคมีอาหาร. สารพิษ 2013, 57, 99 105- [CrossRef] [PubMed]
- 6. โยชินาริ โอ; ชิโอจิมะ, วาย; Igarashi, K. ฤทธิ์ต้านโรคอ้วนของสารสกัดหัวหอมในหนูแรทที่มีไขมันซัคเกอร์ สารอาหาร 2012, 4,1518 1526- [CrossRef]
- 7. อาคาช, MSH; เรห์แมน เค; Chen, S. Spice plant Allium cepa: ผลิตภัณฑ์เสริมอาหารสำหรับรักษาเบาหวานชนิดที่ 2 โภชนาการ 2014, 30, 1128-1137 [CrossRef] [PubMed]
- 8. วัง ย.; เทียน WX; Ma, XF Inhibitory Effects ของหัวหอม (อัลเลียมซีปา L.) สารสกัดจากการเพิ่มจำนวนของเซลล์มะเร็งและ adipocytes ผ่านการยับยั้งการสังเคราะห์กรดไขมัน เอเชี่ยนแพค เจ. มะเร็ง ก่อนหน้า 2012,13, 5573 5579- [CrossRef] [PubMed]
- 9. ลาย WW; ซู, เซาท์แคโรไลนา; Chueh, เอฟเอส ; เฉิน ปป; ยาง JS ; หลิน, เจพี; เลียน เจซี ; ไจ่, CH; Chung, JG Quercetin ยับยั้งการย้ายถิ่นและการบุกรุกของเซลล์มะเร็งในช่องปากของมนุษย์ SAS ผ่านการยับยั้งเส้นทางการส่งสัญญาณของ NF-kappaB และเมทริกซ์เมทัลโลโปรตีนเนส-2/-9 ต้านมะเร็ง 2013, 33, 1941-1950 [PubMed]
- 10. นิคาสโตร, เอชแอล; รอสส์ แคลิฟอร์เนีย; Milner, JA กระเทียมและหัวหอม: คุณสมบัติป้องกันมะเร็ง โรคมะเร็ง ความละเอียด 2015, 8,181 189- [CrossRef]
- 11. ฟอร์เต้ แอล; ทอร์ริเชลลี พี; โบอานินี, อี.; Gazzano, ม.; รูบินี เค; ฟินี ม.; Bigi, A. คุณสมบัติต้านอนุมูลอิสระและการซ่อมแซมกระดูกของไฮดรอกซีอะพาไทต์ที่ทำหน้าที่ quercetin: การศึกษาการเพาะเลี้ยงเซลล์ร่วมกันในหลอดทดลอง osteoblast-osteoclast-endothelial แอคตาไบโอเมเตอร์ 2016, 32, 298 308- [CrossRef]
- 12. ยามาซากิ ย.; อิวาซากิ เค; มิคามิ ม.; ยากิฮาชิ, A. การกระจายสารตั้งต้นรสชาติ XNUMX ชนิด อนุพันธ์ของ S-Alk(en)yl-L-cysteine ในผัก Allium XNUMX ชนิด วิทย์อาหาร. เทคโนโลยี ความละเอียด 2011, 17, 55 62- [CrossRef]
- 13. Block, E. เคมีออร์กาโนซัลเฟอร์ของสกุล Allium—ผลกระทบต่อเคมีอินทรีย์ของกำมะถัน แองเจิ้ล. เคมี. อินเตอร์ เอ็ด อังกฤษ 1992, 31, 1135-1178 [CrossRef]
- 14. กริฟฟิธส์ จี; ทรูแมน, ล.; คราวเธอร์ ที.; โทมัส บี; Smith, B. Onions-ประโยชน์ระดับโลกต่อสุขภาพ ไฟโตเธอร์. ความละเอียด 2002,16, 603 615- [CrossRef]
- 15. ชวิมเมอร์ เอส; Weston, WJ การพัฒนาเอนไซม์ของกรดไพรูวิคในหัวหอมเพื่อวัดความเผ็ดร้อน เจ. อากริก. เคมีอาหาร. 1961, 9, 301 304- [CrossRef]
- 16. เคตเตอร์ กสท; Randle, WM การประเมินความเป็นพิษในหัวหอม ใน การศึกษาทดสอบสำหรับการสอนในห้องปฏิบัติการ; คาร์เชอร์ เอสเจ เอ็ด; Association for Biology Laboratory Education (ABLE): New York, NY, USA, 1998; เล่มที่ 19 หน้า 177-196.
- 17. Hanelt, P อนุกรมวิธาน วิวัฒนาการ และประวัติศาสตร์ ใน หัวหอมและพืชผลที่เกี่ยวข้อง, ฉบับที่. I. พฤกษศาสตร์ สรีรวิทยาและพันธุศาสตร์; Rabinowitch, HD, บรูว์สเตอร์, JL, Eds.; CRC Press: โบคา ราตัน, ฟลอริดา, สหรัฐอเมริกา, 1990; หน้า 1-26.
- 18. ราบิโนวิช เอชดี; คูราห์, แอล. Allium Crop Science: ความก้าวหน้าล่าสุด; สำนักพิมพ์ CABI: Wallingford, UK, 2002
- 19. มายอร์ ซี; คาร์ราเวโด ม.; เอสโตปานัน, G.; Mallor, F. ลักษณะของทรัพยากรพันธุกรรมของหัวหอม (อัลเลียมซีปา L.) จากศูนย์ความหลากหลายทุติยภูมิของสเปน ช่วง เจ. อกริก. ความละเอียด 2011, 9, 144-155 [CrossRef]
- 20. เฟริโอลี เอฟ.; D'Antuono, LF การประเมินฟีนอลิกและซิสเทอีนซัลฟอกไซด์ในหัวเชื้อหัวหอมและหอมแดงในท้องถิ่นจากอิตาลีและยูเครน เจเนท. ทรัพยากร Crop Evol. 2016, 63, 601 614- [CrossRef]
- 21. เปโตรปูลอส, เซาท์ออสเตรเลีย; เฟอร์นานเดส, อ.; บาร์รอส, แอล; เฟอร์ไรร่า, ICFR; Ntatsi, G. คำอธิบายทางสัณฐานวิทยา คุณค่าทางโภชนาการ และทางเคมีของ 'vatikiotiko' ซึ่งเป็นพันธุ์พื้นเมืองของหัวหอมจากกรีซ เคมีอาหาร. 2015,182, 156-163 [CrossRef]
- 22. ลิกัวรี แอล; อดิเลตตา จี; นาซซาโร, ฉ.; Fratianni, F.; ดิ มัตเตโอ ม.; Albanese, D. คุณสมบัติทางชีวเคมี, สารต้านอนุมูลอิสระและฤทธิ์ต้านจุลชีพของหัวหอมพันธุ์ต่างๆ ในพื้นที่เมดิเตอร์เรเนียน เจอาหารตวง. ตัวละคร 2019,13, 1232-1241 [CrossRef]
- 23. ยู แคนซัส; ไพค์, แอล; ครอสบี, เค; โจนส์ อาร์; Leskovar, D. ความแตกต่างของความฉุนของหัวหอมเนื่องจากพันธุ์ สภาพแวดล้อมการเจริญเติบโต และขนาดหัว วิทย์ ฮอร์ติค. 2006,110, 144-149 [CrossRef]
- 24. บีสค์, น.; เพอร์เนอร์, เอช; ชวาร์ซ, ด.; จอร์จ อี.; Kroh, LW; Rohn, S. การแพร่กระจายของ quercetin-3, 4′-O-diglucoside, quercetin-4′-O-monoglucoside และ quercetin ในส่วนต่างๆ ของหัวหอม (Allium cepa L.) ที่ได้รับอิทธิพลจากจีโนไทป์ เคมีอาหาร. 2010,122, 566 571- [CrossRef]
- 25. คารูโซ จี; คอนติ เอส; วิลลารี, จี; บอร์เรลลี ซี; เมลชิออนนา จี; มินูโทโล ม.; รุสโซ, G.; Amalfitano, C. ผลของเวลาในการย้ายปลูกและความหนาแน่นของพืชต่อผลผลิต คุณภาพ และปริมาณสารต้านอนุมูลอิสระของหัวหอม (อัลเลียมซีปา L.) ทางตอนใต้ของอิตาลี วิทย์ ฮอร์ติค. 2014,166, 111-120 [CrossRef]
- 26. เปเรซ-เกรกอริโอ, MR; เรเกอิโร เจ; Simal-Gandara, J.; โรดริเกซ, อาแอส ; Almeida, DPF การเพิ่มมูลค่าเพิ่มของหัวหอมในฐานะแหล่งสารต้านอนุมูลอิสระฟลาโวนอยด์: บทวิจารณ์ที่สำคัญ crit รายได้อาหารวิทย์ Nutr 2014, 54,1050 1062- [CrossRef] [PubMed]
- 27. โพห์นล์, ที.; Schweggert, RM; Carle, R. ผลกระทบของวิธีการเพาะปลูกและการเลือกพันธุ์ต่อคาร์โบไฮเดรตที่ละลายน้ำได้และหลักการฉุนในหัวหอม (อัลเลียมซีปา ล.). เจ. อากริก. เคมีอาหาร. 2018, 66, 12827-12835 [CrossRef] [PubMed]
- 28. เทเดสโก, I.; คาร์โบน, V.; Spagnuolo, ซี; มินาซี พี; Russo, GL การจำแนกและการหาปริมาณของฟลาโวนอยด์จากสองสายพันธุ์ทางตอนใต้ของอิตาลี Allium cepa L., Tropea (หัวหอมแดง) และ Montoro (หัวหอมทองแดง) และความสามารถในการปกป้องเม็ดเลือดแดงของมนุษย์จากความเครียดจากปฏิกิริยาออกซิเดชั่น เจ. อากริก. เคมีอาหาร. 2015, 63, 5229 5238- [CrossRef]
- 29. วิลลาโน, ซี; เอสโปซิโต เอส; คารุชชี, เอฟ; ฟรุสซิอานเต, ล.; คาร์ปูโต, D.; Aversano, R. การสร้างจีโนไทป์ปริมาณงานสูงในหัวหอมเผยให้เห็นโครงสร้างของความหลากหลายทางพันธุกรรมและ SNP ที่ให้ข้อมูลที่เป็นประโยชน์สำหรับการผสมพันธุ์ระดับโมเลกุล โมล พันธุ์. 2019, 39, 5 [CrossRef]
- 30. เมอร์คาติ เอฟ.; ลองโก ซี; โพมา, ด.; อรนิธิ, เอฟ.; ลูปินี, อ.; มัมมะโน, มม; ฟิออเร เอ็มซี; อเบนาโวลี หม่อมราชวงศ์; Sunseri, F การเปลี่ยนแปลงทางพันธุกรรมของมะเขือเทศอายุการเก็บรักษานานของอิตาลี (มะเขือม่วง L.) การรวบรวมโดยใช้ SSR และลักษณะผลไม้ทางสัณฐานวิทยา เจเนท. ทรัพยากร Crop Evol. 2014, 62, 721 732- [CrossRef]
- 31. กอนซาเลซ-เปเรซ เอส; มายอร์ ซี; การ์ซ-เคลเวอร์, อ.; เมอริโน ฉ.; ทาโบอาดา, อ.; ริเวร่า, อ.; โพมาร์ เอฟ.; Perovic, D.; Silvar, C. สำรวจความหลากหลายทางพันธุกรรมและลักษณะคุณภาพในคอลเลกชันของหัวหอม (อัลเลียมซีปา L.) ทางบกจากทางตะวันตกเฉียงเหนือของสเปน พันธุศาสตร์ 2015, 47, 885 900- [CrossRef]
- 32. ลอตตี ซี.; Iovieno, P.; เซ็นโตมานี, I.; มาร์โคตริจิอาโน, เออาร์ ; Fanelli, V.; มิมิโอลา จี; ซัมโม่ ซี; ปาวัน, ส.; Ricciardi, L. ลักษณะทางพันธุกรรม ชีวปฐพีวิทยา และคุณค่าทางโภชนาการของคะน้า (Brassica oleracea แอล. วาร์. อะเซฟาลา) หลากหลายใน Apulia ทางตอนใต้ของอิตาลี ความหลากหลาย 2018,10, 25 [CrossRef]
- 33. บาร์ดาโร, น.; มาร์โคตริจิอาโน, เออาร์ ; Bracuto, V.; มาซเซโอ, ร.; Ricciardi, F.; ล็อตติ, ซี; ปาวัน, ส.; Ricciardi, L. การวิเคราะห์ทางพันธุกรรมของการดื้อต่อ Orobanche เครนาตา (ส้อม.) ในถั่ว (ปิสุมสติวุม L.) สายสตริโกแลคโตนต่ำ. เจ.แพลนท์พาทอล. 2016, 98, 671 675-
- 34. วาโกะ ท.; สึกาซากิ เอช.; ยางุจิ เอส; ยามาชิตะ, เค; อิโตะ เอส; Shigyo, M. การทำแผนที่ของตำแหน่งลักษณะเชิงปริมาณสำหรับเวลาในการมัดหัวหอม (อัลเลียม ฟิสทูโลซัม ล.). ยูไฟติกา 2016, 209, 537 546- [CrossRef]
- 35. ธากา, นิวยอร์ก; มุกโคปะทาย, อ.; Paritosh, K.; คุปตะ, V.; เพนทาล, ง.; Pradhan, AK การระบุ SSRs พันธุกรรมและการสร้างแผนผังการเชื่อมโยงตาม SSR ใน บราซิกา จุนเซีย ยูไฟติกา 2017, 213, 15 [CrossRef]
- 36. อนันธัน, ส.; โมทย์ อาร์; Gopal, J. การประเมินเอกลักษณ์พันธุ์หัวหอมโดยใช้เครื่องหมาย SSR วิทยาศาสตร์เมล็ดพันธุ์ เทคโนโลยี 2014, 42, 279 285- [CrossRef]
- 37. มิโทรวา เค; สโวโบดา พี; Ovesna, J. การเลือกและการตรวจสอบชุดเครื่องหมายสำหรับความแตกต่างของพันธุ์หัวหอมจากสาธารณรัฐเช็ก เช็กเจเจเนท. พันธุ์พืช. 2015, 51, 62 67- [CrossRef]
- 38. ดิ ริเอนโซ, V.; มิอาซซี่, MM; Fanelli, V.; ซาเบ็ตต้า ว.; Montemurro, C. การอนุรักษ์และศึกษาลักษณะความหลากหลายทางชีวภาพของเชื้อพันธุ์มะกอก Apulian แอ็กต้าฮอร์ติค. 2018,1199,1 6- [CrossRef]
- 39. มายอร์ ซี; อาร์เนโด-อันเดรส, อ.; Garces-Claver, A. การประเมินความหลากหลายทางพันธุกรรมของชาวสเปน Allium cepa Landraces สำหรับการเพาะพันธุ์หัวหอมโดยใช้เครื่องหมายไมโครแซทเทลไลท์ วิทย์ ฮอร์ติค. 2014,170, 24-31 [CrossRef]
- 40. ริเวร่า อ.; มายอร์ ซี; การ์ซ-เคลเวอร์, อ.; การ์เซีย-อูลัว, อ.; โพมาร์ เอฟ.; Silvar, C. การประเมินความหลากหลายทางพันธุกรรมของหัวหอม (Allium cepa L.) ทางบกจากทางตะวันตกเฉียงเหนือของสเปนและเปรียบเทียบกับความแปรปรวนของยุโรป พืชสวน NZJ 2016, 44, 103-120 [CrossRef]
- 41. เด จิโอวานนี่ ซี; ปาวัน, ส.; ทารันโต, ฉ.; Di Rienzo, V.; มิอาซซี่, MM; มาร์โคตริจิอาโน, เออาร์ ; Mangini, G.; มอนเตมูร์โร ซี; Ricciardi, L.; Lotti, C. การเปลี่ยนแปลงทางพันธุกรรมของการรวบรวมเชื้อโรคทั่วโลกของถั่วชิกพี (ไซเซอร์ arietinum L.) รวมถึงการภาคยานุวัติของอิตาลีที่เสี่ยงต่อการพังทลายของพันธุกรรม ฟิสิโอล โมล ไบโอล พืช 2017, 23, 197-205 [CrossRef]
- 42. มาซเซโอ ร.; มอร์เกส, อ.; Sonnante, G.; ซูลูอากา, ดีแอล ; ปาวัน, ส.; Ricciardi, L.; Lotti, C. ความหลากหลายทางพันธุกรรมในผักชนิดหนึ่ง (บราสสิก้าราปา ล. ย่อย ซิลเวสทริส (ล.) Janch.) จากอิตาลีตอนใต้. วิทย์ ฮอร์ติค. 2019, 253, 140-146 [CrossRef]
- 43. จักรเซ่ ม.; มาร์ติน ว.; แมคคอลลัม เจ; Havey, M. Single nucleotide polymorphisms, indels และลำดับอย่างง่ายซ้ำสำหรับการระบุพันธุ์หัวหอม แยม. สังคม ฮอร์ติค. วิทย์ 2005,130, 912 917- [CrossRef]
- 44. แมคคัลลัม เจ; ทอมสัน เอส.; พิเธอร์-จอยซ์ ม.; Kenel, F. การวิเคราะห์ความหลากหลายทางพันธุกรรมและการพัฒนาเครื่องหมาย single-nucleotide polymorphism ในหัวหอมใหญ่ที่ปลูกโดยอิงตามเครื่องหมายลำดับซ้ำแท็กลำดับง่ายๆ แยม. สังคม ฮอร์ติค. วิทย์ 2008,133, 810 818- [CrossRef]
- 45. บอลด์วิน เอส; พิเธอร์-จอยซ์ ม.; ไรท์ เค; เฉิน, ล.; McCallum, J. การพัฒนาเครื่องหมายทำซ้ำลำดับจีโนมแบบง่ายที่มีประสิทธิภาพสำหรับการประมาณค่าความหลากหลายทางพันธุกรรมภายในและระหว่างหัวหอมใหญ่ (อัลเลียมซีปา L.) ประชากร. โมล พันธุ์. 2012, 30, 1401-1411 [CrossRef]
- 46. เดอวู้ดดี้ จา; ฮันนี่คัต, RL; Skow, LC Microsatellite markers ในกวางหางขาว เจ. เฮิร์ด. 1995, 86, 317 319- [CrossRef] [PubMed]
- 47. คบดาดี ม.; Hassanpanah, D. หัวหอมอิหร่าน (อัลเลียมซีปา L.) พันธุ์ตอบสนองต่อภาวะซึมเศร้าทางสายเลือด แอพพลิเคชั่นระดับโลก วิทย์ เจ 2010,11, 426 428-
- 48. อับดู ร.; บากัสโซ่, ย.; ซาดู ม.; โบดวง, JP; Hardy, OJ ความหลากหลายทางพันธุกรรมของหัวหอมไนเจอร์ (อัลเลียมซีปา L.) ประเมินโดยเครื่องหมายทำซ้ำลำดับอย่างง่าย (SSR) แอ็กต้าฮอร์ติค. 2016,1143, 77 90- [CrossRef]
- 49. ภาวัน ส.; ล็อตติ, ซี; มาร์โคตริจิอาโน, เออาร์ ; มาซเซโอ, ร.; บาร์ดาโร, น.; Bracuto, V.; Ricciardi, F.; ทารันโต, ฉ.; D'Agostino, N.; สเคียวัลลี, อ.; และอื่น ๆ กลุ่มพันธุกรรมที่แตกต่างกันในถั่วชิกพีที่ปลูกซึ่งเปิดเผยโดยการค้นพบเครื่องหมายทั้งจีโนมและการสร้างจีโนไทป์ จีโนมพืช 2017, 2017,10. [CrossRef]
- 50. ภาวัน ส.; มาร์โคตริจิอาโน, เออาร์ ; Ciani, อี.; มาซเซโอ, ร.; ซอนโน, V.; Ruggieri, V.; ล็อตติ, ซี; Ricciardi, L. การจำแนกจีโนไทป์ตามลำดับของแตงโม (เมล่อนแตงกวา L. ) การรวบรวมเชื้อโรคจากศูนย์ทุติยภูมิของความหลากหลายเน้นรูปแบบความผันแปรทางพันธุกรรมและคุณลักษณะจีโนมของกลุ่มยีนต่างๆ BMC จีโนม 2017, 18, 59 [CrossRef]
- 51. ดิ ริเอนโซ, V.; ไซออน เอส; ทารันโต, ฉ.; D'Agostino, N.; มอนเตมูร์โร ซี; Fanelli, V.; ซาเบ็ตต้า ว.; บูเชฟฟา เอส; ทาเมนจารี, อ.; พาสควาโลน, อ.; และอื่น ๆ การถ่ายทอดทางพันธุกรรมของประชากรมะกอกในแอ่งทะเลเมดิเตอร์เรเนียน เพียร์เจ 2018, 6. [CrossRef]
- 52. คนเลี้ยงแกะ, แอลดี; McLay, TG สองโปรโตคอลขนาดเล็กสำหรับการแยก DNA จากเนื้อเยื่อพืชที่อุดมด้วยโพลีแซคคาไรด์ เจ. แพลนท์เรส 2011,124, 311 314- [CrossRef]
- 53. ดอยล์, เจเจ; Doyle, JL การแยก DNA ของพืชออกจากเนื้อเยื่อสด โฟกัส 1990,12, 13-14
- 54. คูห์ล เจซี; Cheung, F.; เฉียวผิง, วาย.; มาร์ติน ว.; Zewdie, Y.; แมคคอลลัม เจ; Catanach, A.; รัทเทอร์ฟอร์ด พี; จม, เคซี; เจนเดอเรค ม.; และอื่น ๆ ชุดแท็กลำดับการแสดงหัวหอม 11,008 ชุดที่ไม่ซ้ำกันเผยให้เห็นลำดับการแสดงและความแตกต่างของจีโนมระหว่างหน่อไม้ฝรั่งและปอ เซลล์พืช 2004,16, 114 125- [CrossRef]
- 55. คิม เอชเจ; ลี ทรัพยากรบุคคล; ฮยอน, JY; เพลง, KH; คิม, เคเอช; คิม, เจ; เฮอร์ CG; หาญ การพัฒนา CH Marker สำหรับการทดสอบความบริสุทธิ์ทางพันธุกรรมของหัวหอมโดยใช้ SSR Finder สายพันธุ์เจเกาหลี. วิทย์ 2012, 44, 421 432- [CrossRef]
- 56. Schuelke, M. วิธีการทางเศรษฐศาสตร์สำหรับการติดฉลากเรืองแสงของชิ้นส่วน PCR แนท. เทคโนโลยีชีวภาพ. 2000, 18, 233 234- [CrossRef] [PubMed]
- 57. พีคอล, ร.; Smouse, PE GenAlEx 6.5: การวิเคราะห์ทางพันธุกรรมใน Excel ซอฟต์แวร์พันธุศาสตร์ประชากรสำหรับการสอนและการวิจัย: การปรับปรุง ชีวสารสนเทศศาสตร์ 2012, 28, 2537 2539- [CrossRef] [PubMed]
- 58. คาลิโนวสกี้ เซนต์; เทเปอร์, ม.ล.; Marshall, TC การแก้ไขวิธีการที่โปรแกรมคอมพิวเตอร์ CERVUS รองรับข้อผิดพลาดในการพิมพ์จีโนไทป์ช่วยเพิ่มความสำเร็จในการกำหนดความเป็นพ่อ มล. อีโคล. 2007,16, 1099-1106 [CrossRef]
- 59. พริทชาร์ด เจ.เค.; สตีเฟนส์ ม.; โรเซนเบิร์ก เอ็นเอ; Donnelly, P. การทำแผนที่สมาคมในประชากรที่มีโครงสร้าง เป็น. เจ. ฮัม. เจเนท. 2000, 67, 170 181- [CrossRef]
- 60. Evanno, G.; Regnaut, เอส; Goudet, J. การตรวจจับจำนวนของกลุ่มบุคคลโดยใช้โครงสร้างซอฟต์แวร์: การศึกษาแบบจำลอง มล. อีโคล. 2005,14, 2611 2620- [CrossRef]
- 61. เอิร์ล, ด.; VonHoldt, B. STRUCTURE HARVESTER: เว็บไซต์และโปรแกรมสำหรับการแสดงภาพผลลัพธ์ของโครงสร้างและการใช้วิธี Evanno อนุรักษ์. เจเนท. ทรัพยากร 2011, 4. [CrossRef]
- 62. ทาเคซากิ น.; เนย ม.; Tamura, K. POPTREEW: POPTREE เวอร์ชันบนเว็บสำหรับสร้างต้นไม้ประชากรจากข้อมูลความถี่อัลลีลและคำนวณปริมาณอื่นๆ โมล จิตเวช. อีโวล. 2014, 31, 1622 1624- [CrossRef]
- 63. มาร์, ส.; Stecher, G.; ลี่ ม.; Knyaz, C.; Tamura, K. MEGA X. การวิเคราะห์พันธุศาสตร์วิวัฒนาการระดับโมเลกุลข้ามแพลตฟอร์มคอมพิวเตอร์ โมล จิตเวช. อีโวล. 2018, 35, 1547-1549 [CrossRef]